
Ім'я файлу: Клиническая_фармакология_учебник.docx
Розширення: docx
Розмір: 1432кб.
Дата: 16.09.2022
скачати
Розширення: docx
Розмір: 1432кб.
Дата: 16.09.2022
скачати
Фармакодинамика лекарственных средств
Фармакодинамика ЛС— это раздел клинической фармакологии, изучающий механизмы действия, характер, силу и длительность фармакологических эффектов ЛС у человека.
Фармакологический эффект — это изменение функции (-й) на всех уровнях (от субклеточного до организменного) под воздействием лекарственных средств.
В организме молекулы ЛС взаимодействуют с функционально значимыми молекулами (первичная фармакологическая реакция), что приводит к развитию фармакологического эффекта. Функционально значимые молекулы (молекулярный субстрат или молекулярные мишени действия ЛС) — это белки, нуклеиновые кислоты, фосфолипиды и др., которые входят в состав рецепторов, ферментов, ионных каналов, сократительных белков и т.п. Рецепторы могут входить в состав цитоплазматической мембраны либо представляют собой растворимые внутриклеточные рецепторы (в частности, для тиреоидных и стероидных гормонов). Около 80 % рецепторов относят к рецепторам первого типа. Это опиоидные, α- и β-адрено-, М-холинорецепторы и др., сопряженные с G-белками. Медиаторы (лиганды, биорегуляторы) взаимодействуют с этими рецепторами, что приводит к активации G-белков. Затем происходит стимуляция или инактивация различных эффекторных систем (аденилатциклазной, гуанилатциклазной, инозитолфосфатной, ионных каналов). Рецепторами второго типа являются тирозиновые протеинкиназы (например, рецепторы инсулина). Результатом связывания внеклеточного домена этих рецепторов с лигандами является активация внутриклеточного домена. Это приводит к фосфорилированию аминокислотных остатков тирозина в различных регуляторных белках. Катионные и анионные каналы (Н-холино-, глициновые и другие рецепторы) — это рецепторы третьего типа. При связывании лигандов с мембранными белками происходит изменение проницаемости мембраны для различных ионов. Вследствие этого изменяется мембранный потенциал или внутриклеточная концентрация различных ионов. Растворимые внутриклеточные рецепторы представляют собой четвертый тип рецепторов.
При взаимодействии (химическом или физико-химическом) молекул ЛС с функционально значимыми молекулами организма происходит изменение конформации определенных участков молекулы рецептора. При этом повышается, понижается или полностью подавляется функция клеток, органов и систем. Врачу важно знать не только уровень изменения этой функции, но и в каком направлении изменяется функция клеток, органов и систем:
* повышается сниженная функция до нормы (тонизирующее действие);
* повышается функция сверх нормы (возбуждающее действие);
* понижается избыточная функция до нормы (седативное действие);
* понижается функция ниже нормы (угнетающее действие);
* полностью подавляется функция (парализующее действие).
Некоторые ЛС повышают или угнетают активность специфических ферментов. Например, физостигмин или неостигмин снижает активность холинэстеразы, разрушающей ацетилхолин, и проявляет эффекты, характерные для возбуждения парасимпатической нервной системы. Фенобарбитал, повышая активность глюкуронилтрансферазы печени, снижает уровень билирубина в крови.
Деятельность клеток нервной и мышечной систем зависит от потоков ионов, определяющих трансмембранный электрический потенциал. Некоторые ЛС изменяют транспорт ионов. Так действуют антиаритмические, противосудорожные препараты, средства для общего наркоза.
ЛС могут непосредственно взаимодействовать с небольшими молекулами или ионами внутри клеток. Например, этилендиаминтетрауксусная кислота прочно связывает ионы свинца.
Избирательность (селективность) действия
Избирательность (селективность) действия ЛС заключается в том, что они способны изменять функцию одних клеток, органов и систем, не изменяя при этом функцию других. Изменение функции зависит от наличия в клетках молекулярного субстрата действия ЛС. Если нет молекулярного субстрата, нет и действия. ЛС в силу своей природы могут не проникать в эти молекулярные мишени, например, в клетки мозга из-за наличия гематоэнцефалического барьера. Таким образом, избирательность действия ЛС определяется их фармакодинамикой и фармакокинетикой.
Вещества с низкой избирательностью действия оказывают влияние на многие ткани, органы и системы, вызывая множество побочных реакций. Так, противоопухолевые средства, действуя на быстроделящиеся клетки, повреждают не только ткань опухоли, но и костный мозг, эпителий кишечника. Однако имеются препараты с относительно высокой избирательностью действия (блокаторы Н1-, Н2-гистаминовых рецепторов, β1-адреноблокаторы, β2-адреномиметики).
Избирательность действия лекарственного препарата зависит от его дозы. Чем выше доза препарата, тем меньше избирательность. Это относится и к синтетическим веществам, и к продуктам животного и растительного происхождения. Например, антидиуретический гормон гипофиза (вазопрессин) регулирует содержание жидкости в организме, оказывая влияние на реабсорбцию воды в почках. Однако в больших дозах он может вызвать спазм кровеносных сосудов, в том числе коронарных, и даже смерть больного.
В то же время изменение функции клеток (органов и систем) может осуществляться не за счет прямого действия ЛС (например, при отсутствии молекулярного субстрата), а вследствие непрямого (косвенного) действия, опосредованного анатомо-физиологическими взаимоотношениями у этих клеток или органов. Наиболее известный пример непрямого действия — рефлекторное действие ЛС, когда раздражение афферентных нервных окончаний (в коже, слизистых) приводит к изменению функции клеток органа, отдаленного от места первичного действия ЛС.
Фармакокинетика лекарственных средств
Фармакокинетика— это раздел клинической фармакологии, изучающий пути введения, биотрансформацию, связи с белками крови, распределение и выведение ЛС.
При фармакокинетическом изучении ЛС измеряют его концентрацию в биологических средах (кровь, моча, слизь и т.д.) в определенные моменты времени. Частота и продолжительность забора биологических проб зависит от продолжительности пребывания лекарственного вещества или его метаболитов в организме. Концентрацию препаратов определяют с помощью жидкостной или газожидкостной хроматографии, радиоиммунного анализа или ферментно-химического анализа, полярографии, спектрофотометрии и т.д. На основании полученных данных строится график (рис. 1.1). Кривая концентрация—время характеризует процессы, происходящие с исследуемым препаратом.
Изменения, которым подвергаются ЛС в организме и их экскреция, определяют их судьбу.
Изменение лекарственного вещества в живом организме называется биотрансформацией.
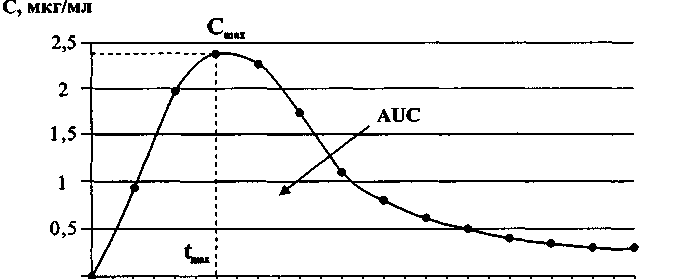
Рис. 1.1. Основные параметры фармакокинетики: Сmах— максимум или пик концентрации лекарственного вещества в крови; tmах — время достижения максимальной концентрации лекарственного вещества; АUС — площадь под фармакокинетической кривой (изменение концентрации активного вещества в плазме или сыворотке крови во времени)
После всасывания препараты могут метаболизироваться под влиянием ферментов, изменяться спонтанно, превращаясь в другие вещества без воздействия ферментов, либо могут экскретироваться в неизмененном виде. В процессе метаболизма ЛС, как правило, из веществ с низкой полярностью и растворимых в жирах превращаются в вещества более поляризованные и водорастворимые, в результате чего облегчается их экскреция почками. Если лекарственное вещество поляризовано и хорошо растворимо в воде, оно экскретируется, не подвергаясь метаболизму. Многие ЛС, не метаболизирующиеся в организме, представляют собой вещества высокополяризованные (например, метотрексат). Однако большинство лекарственных веществ метаболизируются под воздействием ферментов, в результате чего они активируются, инактивируются или модифицируются. При этом в организме происходят окисление, восстановление, гидролиз и синтез (конъюгация, или реакция переноса). В процессе окисления, восстановления и гидролиза молекула приобретает полярные группы: гидроксильные, аминные, сульфгидрильные и карбоксильные. В результате лекарственное вещество становится водорастворимым и фармакологически менее или более активным.
Метаболизм ЛС может происходить во многих тканях, но наиболее активной в расчете на единицу массы тела является ткань печени. Ферменты, метаболизирующие ЛС, локализованы в микросомах печеночных клеток. Цитохромы P446-455 (в большинстве случаев по первому обнаруженному ферменту этой системы указывают только цитохром Р450) являются первичными компонентами окислительной ферментной системы. Некоторые ЛС при их повторном введении могут стимулировать микросомальные ферменты печени (например, барбитураты, кофеин, этанол). Это явление называется индукцией ферментов. К Л С, которые подавляют и даже разрушают цитохром P450, относятся ксикаин, совкаин, бенкаин, индерал, вискен.
Все фармакокинетические процессы оказывают влияние на концентрацию ЛС в организме и, в конечном итоге, на величину эффекта ЛС. Концентрацию ЛС в крови, вызывающую эффект, равный 50 % максимального (ЕС50), определяют как минимальную терапевтическую концентрацию ЛС.
Интервал между минимальной терапевтической концентрацией ЛС и концентрацией, вызывающей появление первых признаков токсического действия, называется терапевтическим диапазоном (терапевтическим окном, коридором безопасности).
Отношение же концентрации верхней границы терапевтического диапазона к концентрации нижней границы определяют как терапевтическую широту ЛС. Среднее значение терапевтической широты представляет собой среднюю терапевтическую концентрацию.
Всасывание (абсорбция) ЛС — это поступление его с места введения в системный кровоток.
Пути введения ЛС следующие:
* энтеральные (через ЖКТ) — оральный, ректальный, сублингвальный;
* парентеральные (минуя ЖКТ) — внутримышечный, внутривенный, внутриартериальный, подкожный, трансдермальный, ингаляционный и др.
Энтеральный путь введения используется наиболее часто. Его достоинства — безопасность, удобство использования, экономическая выгода и отсутствие осложнений, типичных для парентерально применяемых препаратов.
При энтеральных способах введения ЛС всасываются относительно медленно. На абсорбцию в ЖКТ оказывают влияние:
*физико-химические свойства ЛС и лекарственной формы (водо- и жирорастворимость, константа диссоциации, молекулярная масса);
* состояние функций ЖКТ (рН, ферменты, состав желудочного и кишечного соков, скорость опорожнения желудка, патологические процессы в ЖКТ, возраст пациента, скорость мезентериального кровотока, прием пищи и др.);
* фармакокинетические факторы (взаимодействие с другими ЛС, метаболизм в стенке кишечника и под действием микрофлоры и др.).
Всасывание ЛС при энтеральных способах введения в отличие от парентеральных весьма вариабельно и непостоянно. Это иногда приводит к затруднениям в выборе режима дозирования. Не только патологические процессы в ЖКТ, но и болевой синдром, снижение системного АД, кровотечение способствуют снижению абсорбции ЛС из ЖКТ.
При сублингвальном применении ЛС должно полностью раствориться в полости рта. Активное вещество поступает непосредственно в системный кровоток, минуя систему воротной вены (т.е. не разрушается в печени). Достоинства этого метода введения — быстрое начало действия, быстрое прекращение действия при извлечении препарата из полости рта, предотвращение разрушения части препарата ферментами ЖКТ.
Достоинствами парентерального метода являются возможность введения ЛС больным, находящимся без сознания, неконтактным больным, при рвоте, диарее, а также больным, у которых нарушен акт глотания; ЛС не подвергаются воздействию ферментов ЖКТ.
При внутривенном и внутриартериальном способах введения ЛС поступает в системный кровоток сразу; в остальных случаях этому предшествует фаза всасывания. Всасывание может осуществляться посредством пассивной диффузии, фильтрации, активного транспорта, облегченного транспорта, пиноцитоза. Чаще имеет место сочетание большей части этих механизмов, однако может преобладать один из них, что зависит от способа введения и физико-химических свойств ЛС (не растворимые в средах организма ЛС не всасываются).
При внутривенном способе введения ЛС вся доза попадает в системный кровоток, что может обеспечить более быстрое и полное поступление его в места первичного действия, т.е. биофазу; действие ЛС развивается быстро, обычно через 2-3 мин.
При подкожном и внутримышечном введении ЛС из межклеточного пространства путем диффузии и фильтрации в капилляры поступает в общий кровоток; действие ЛС развивается через 10-15 мин.
Введение ЛС методом внутриартериальных инъекций применяется для диагностических целей (проведение ангиографии) или при введении цитостатиков для перфузии новообразования.
Интратекальное введение — это введение ЛС в субарахноидальное пространство.
При этом вещества воздействуют непосредственно на ЦНС. Этот путь используется для проведения спинальной анестезии или в случае необходимости создания высоких концентраций препаратов в субарахноидальном пространстве (например, антибиотиков, глюкокортикоидов).
При попадании в системный кровоток (или лимфатические протоки) ЛС в большей или меньшей степени связывается с белками, что оказывает влияние на фармакокинетику и фармакодинамику, так как связанное с белком ЛС не взаимодействует с рецепторами, ферментами, не проникает через мембраны. По мере насыщения способность белков связывать ЛС уменьшается. Уменьшение количества связывающих белков плазмы крови на 10-15 % отмечается при старении организма. Изменение уровня связывания ЛС с белком наблюдается при их конкуренции за связь с белком, когда более активные вещества вытесняют вещества, имеющие меньшее сродство к этим белкам. Терапевтический эффект зависит от концентрации свободной фракции; при заболеваниях печени и почек концентрация несвязанной формы вещества может увеличиваться. В этом случае иногда приходится уменьшать дозу препарата или кратность его введения.
Распределение лекарственных средств — это процесс его поступления из системного кровотока в межклеточную жидкость и внутрь клетки.
Вещества с высокой молекулярной массой (например, поливинилпирролидон) не способны проходить через поры капилляров. На распределение ЛС оказывает влияние состояние гемодинамики, так как ее нарушение, например, при сердечной недостаточности, уменьшает перфузию органов. Уменьшение, в частности, почечного кровотока ведет к нарушению гломерулярной фильтрации и соответственно к снижению почечного клиренса. В результате концентрация ЛС, особенно после внутривенного введения, возрастает.
Выведение ЛС (или его метаболитов) из организма осуществляется почками (чаще), легкими, через ЖКТ с фекалиями, а также потовыми, слюнными, слезными и молочными железами. О выведении ЛС из организма судят по периоду полувыведения (Т1/2). Период полувыведения — это период в течение которого концентрация Л С в плазме крови уменьшается на 50 %.
Совокупность процессов биотрансформации и выведения лекарственных средств называется элиминацией.
Элиминация ЛС может осуществляться в процессе всасывания в систему кровотока. Это наблюдается при оральном, внутримышечном, подкожном и других путях введения. В таком случае говорят о пресистемной элиминации.
Выраженность действия ЛС в большей степени коррелирует с их концентрацией в крови и тканях. На содержание препарата в крови оказывают влияние многие факторы (биодоступность, состояние печени и почек и т.п.), поэтому у больных, получающих ЛС в одной и той же дозе, его концентрация в крови может оказаться различной. Особенно трудно предсказать возможную концентрацию ЛС в крови в таких случаях, как:
* лихорадка;
* наличие сопутствующей патологии;
* использование препаратов в необычных дозах;
* нарушение всасывания и низкая биодоступность;
* применение препаратов, взаимодействующих между собой;
* генетически обусловленные особенности метаболизма препаратов.
В подобных ситуациях концентрация препарата может оказаться слишком низкой или слишком высокой. В первом случае снижается эффективность лечения, во втором — повышается риск побочных реакций. При применении некоторых ЛС возникает необходимость в их терапевтическом мониторинге, т.е. регулярном определении концентрации в крови. При отборе ЛС для терапевтического мониторинга учитывают следующие факторы: небольшую широту терапевтического действия препарата, нелинейную фармакокинетику, большой объем распределения, необходимость длительной терапии, применение ЛС при угрожающих жизни состояниях.
Содержание ЛС определяют с помощью иммуноферментных, иммунофлуоресцентных, спектрометрических методов, позволяющих за несколько минут получить необходимую информацию.
Факторы, оказывающие влияние на действие и применение лекарственных средств
Известно большое количество факторов, изменяющих фармакодинамику, а также фармакокинетику ЛС. Из множества этих факторов следует отметить дозу ЛС, пути его введения в организм, кратность применения, массу тела, пол, возраст, индивидуальные особенности (чувствительность и др.), характер питания и др.
Как правило, чем выше доза ЛС (соответственно концентрация), тем выше фармакологический эффект. Однако при увеличении дозы фармакологический эффект может изменяться не только количественно, но и качественно. Например, при введении этилового спирта малые дозы вызывают возбуждение, а большие — состояние наркоза и даже смерть. Выделяют терапевтические, токсические и летальные дозы. Для врача имеют значение разовые (количество вещества, предназначенного на один прием), суточные и курсовые дозы. Существует понятие максимальной терапевтической дозы, превышение которой опасно для больного.
Безопасность ЛС характеризуется отношением средней летальной дозы к средней терапевтической (LD50/ED50) — терапевтическим индексом. Чем выше значение этого индекса, тем безопаснее ЛС.
При многократном применении ЛС его действие может изменяться в результате:
* кумуляции (материальной либо функциональной);
* сенсибилизации (повышение чувствительности к повторному введению);
* привыкания (толерантности) — уменьшения эффекта при повторном введении);
* пристрастия (лекарственной зависимости — психической и/или физической).
В случае длительного применения ЛС, медленно экскретирующихся, происходит повышение их концентрации в организме. Чтобы избежать кумуляции, следует знать время элиминации лекарственных веществ, прекратить применение препарата при появлении первых симптомов побочного действия.
Для того, чтобы получить эффект при развитии толерантности к ЛС, требуется постоянно увеличивать дозу препарата. Толерантность к ЛС бывает двух типов:
* истинная (врожденная или приобретенная);
* относительная (псевдотолерантность).
Истинная врожденная толерантность наблюдается у некоторых рас. Инсталляция раствора эфедрина в конъюнктивальный мешок вызывает быстрое расширение зрачка у коренных жителей Кавказа, а у лиц негроидной расы расширение зрачка вообще может не наступить.
Истинная приобретенная толерантность возникает при повторном (многократном) введении препарата. Толерантность развивается к различным препаратам, в том числе к барбитуратам, опиатам, нитратам, ксантинам и др. Иногда в клинике толерантность может быть желательной. Так, у больных эпилепсией при лечении барбитуратами развивается толерантность к снотворному действию, а противоэпилептический эффект не изменяется. Однако в целом толерантность нежелательна.
Относительная толерантность проявляется только при введении препаратов внутрь. В средние века, опасаясь отравления, часто принимали внутрь небольшие дозы ядов. Это приводило к развитию устойчивости к ядам, поступающим лишь этим путем, но не защищало от действия яда, если он поступал в организм иным путем. Такой вид толерантности, вероятно, обусловлен иммунологическими процессами в ЖКТ, предупреждающими всасывание препаратов.
Повторное применение некоторых препаратов может приводить к развитию привыкания и лекарственной зависимости. Если прекратить прием вещества, к которому развилось привыкание, у человека появляется синдром отмены (абстиненции), характеризуемый нарушениями психики. ВОЗ определяет лекарственную зависимость как "состояние психики и иногда и физическое состояние человека, являющееся следствием взаимодействия живого организма с лекарственным средством и характеризуемое определенными поведенческими и другими реакциями, в число которых входит потребность принимать препарат в течение длительного времени или эпизодически, чтобы получить эффект в отношении психики, а иногда, чтобы избежать дискомфорта при отсутствии препарата в организме ".
Состояние, при котором лекарственное средство вызывает чувство удовлетворения и такое состояние психики, которое требует периодического или длительного применения препарата, называется психической зависимостью. При физической зависимости организм достигает такого адаптивного состояния, которое проявляется тяжелыми физическими нарушениями в случае отмены препарата. Тяжелую физическую и психическую зависимость вызывают опиаты и морфиноподобные препараты, алкоголь, барбитураты и др. Препараты, вызывающие выраженную психическую, но незначительную физическую зависимость, — это антагонисты опиатов, фенаминоподобные средства (фенамин, метфенамин). К препаратам, вызывающим только психическую зависимость относятся кокаин, ЛСД, никотин, кофеин.
Факторы, изменяющие эффекты лекарственных веществ, — это возраст, масса тела, пол пациента, генетические факторы, время приема, взаимодействие с пищей и др.
Возраст — один из основных факторов, учитываемый при дозировании ЛС. Дозы, приведенные в Фармакопее, рассчитаны для лиц 20-60 лет; соответственно больным, моложе 20 и старше 60 лет назначают часть указанных доз. Такой подход к дозированию ЛС объясняется тем, что масса тела у детей ниже, чем у взрослых, следовательно, объем распределения ЛС меньше. У пожилых людей ткани организма хуже удерживают воду, что также способствует уменьшению объема распределения. У молодых и пожилых ниже активность ферментов, принимающих участие в биотрансформации ЛС, что приводит к увеличению периода полужизни препарата. Функции почек новорожденных еще несовершенны, а у пожилых снижены из-за уменьшения количества функционирующих нефронов, что замедляет процесс выведения ЛС.
Масса тела. Средняя доза обычно выражается в миллиграммах на килограмм массы тела либо в общей суточной дозе для взрослого с массой тела 60-90 кг (в среднем 70 кг). Однако такое дозирование может быть неадекватным для больных с ожирением, а также для больных с отеками, обезвоженных или истощенных.
Пол.Средства, угнетающие ЦНС, такие как морфин и барбитураты, могут иногда вызывать состояние возбуждения у женщин. С особым вниманием следует назначать ЛС во время беременности, лактации. Реакция грудного молока более кислая, чем плазмы крови, поэтому ЛС со свойствами слабых оснований, которые становятся более ионизированными при уменьшении рН, могут появляться в молоке в концентрациях, равных их концентрации в плазме крови, или более высоких.
В менструальный период следует избегать применения ЛС, усиливающих кровенаполнение органов малого таза, антиагрегантов, антикоагулянтов.
Характерологические особенности личности (эмоциональный фактор) также могут влиять на эффекты ЛС.
Действие ЛС может изменяться под влиянием таких физиологических факторов, как кислотно-основное состояние, температура тела, водный и электролитный баланс.
Комбинированное (совместное) использование ЛС может приводить к изменению эффектов препаратов. Обычно выделяют два варианта взаимного влияния ЛС: синергизм и антагонизм.
Синергизм проявляется в тех случаях, когда ЛС содействуют друг другу, т.е. способствуют усилению эффекта. В основе синергизма может лежать влияние одного вещества на фармакокинетику другого: ускорение или замедление всасывания, вытеснение из связи с белком, ингибиция ферментов, принимающих участие в биотрансформации ЛС, замедление выведения. Синергизм также может быть обусловлен фармакодинамическим взаимодействием ЛС. В этом случае ЛС, оказывающие однонаправленное действие, связываются с различными молекулярными субстратами, например при совместном применении α- и β-адреноблокаторов в качестве антигипертензивных ЛС. В этом случае говорят о потенцированном синергизме. Потенцирование — наиболее частая причина использования комбинации ЛС.
Антагонизм — полное устранение или частичное уменьшение эффекта одного ЛС другим. Выделяют физический, химический и функциональный антагонизм. Абсорбция токсинов активированным углем — пример физического антагонизма. Образование неактивного соединения в результате химического взаимодействия ЛС — химический антагонизм.
Функциональный антагонизм реализуется через функциональные системы организма, между собой ЛС не взаимодействуют, а их противодействие реализуется посредством биосубстрата. Функциональный антагонизм используется в практике с целью устранения побочных эффектов ЛС, а также при их передозировке.
При назначении ЛС (и их комбинаций) необходимо учитывать такие факторы, как беременность и кормление грудью. Проникая через плацентарный барьер, ЛС может оказывать действие на плод и вызывать пороки развития, смерть плода, выкидыш, угнетение функций различных его органов и систем. При кормлении грудью ЛС, применяемое матерью, может выделяться с молоком, которое получает новорожденный. Это может стать причиной различных психосоматических изменений у ребенка. Некоторые ЛС могут уменьшать или полностью прекращать лактацию. Как правило, данных о действии препаратов на плод и новорожденного недостаточно, что связано с трудностями этих исследований.
При необходимости назначения медикаментозного лечения матери необходимо соизмерять пользу и вред — потенциальная польза должна превосходить потенциальный вред. Помня о том, что ни одно ЛС не может считаться на 100 % безопасным для плода, по возможности используют препараты, оказывающие наименьшее влияние на плод (или новорожденного). Препараты с выраженным тератогенным или эмбриотоксическим действием не должны назначаться женщинам детородного возраста без строгих показаний и надежной контрацепции.
Важно учитывать, что при беременности фармакокинетика ЛС может изменяться. Это обусловливает соответствующую коррекцию разовой дозы, кратность назначения и, возможно, путь введения лекарства.
Применение ЛС в период беременности может ограничивать наличие у них нежелательных свойств, таких как:
* тератогенное действие —способность ЛС вызывать структурные (уродство) и функциональные дефекты развития плода в период эмбриогенеза (примером может служить "талидомидовая трагедия", при которой отмечалось рождение детей с фокомелией ("тюленьи" конечности) у матерей, принимавших седативный препарат талидомид). Тератогенные аномалии по наследству не передаются;
* мутагенное действие — способность ЛС вызывать стойкое повреждение зародышевой клетки и ее генетического аппарата, которое проявляется в изменении генотипа потомства, т.е. передается по наследству. Мутагенное действие чаще возникает в результате применения ЛС родителями в период гонадо- и/или эмбриогенеза;
* эмбриотоксическое и фетотоксическое действиеЛС не связано с нарушением органогенеза, а расценивается как токсическое действие ЛС. Если такое токсическое действие проявляется в первые 12 недель беременности, говорят об эмбриотоксическом (embrion — зародыш), а в более поздние сроки — о фетотоксическом (fetus — плод) действии.
Эффективность и переносимость одних и тех же ЛС у разных людей может быть неодинакова, что зачастую обусловлено генетическими факторами, определяющими процессы метаболизма ЛС, рецепции, иммунного ответа.
Клиническая фармакогенетика разрабатывает методы диагностики, профилактики и коррекции необычного ответа организма на действие ЛС. Наследственные факторы, определяющие необычный ответ на ЛС, чаще всего являются биохимическими. Так, наличие у некоторых людей атипичной псевдохолинэстеразы способствует развитию длительного паралича дыхательной мускулатуры после введения миорелаксанта дитилина. Недостаточность глюкозо-6-фосфатдегидрогеназы приводит к массивному распаду эритроцитов (гемолитический криз) при назначении противомалярийного препарата примахина. Подобные гемолитические кризы могут также возникать при употреблении отдельных продуктов (конские бобы, крыжовник, красная смородина) у представителей некоторых национальностей (азербайджанцы, греки, афроамериканцы, болгары, арабы, евреи и др.). Такое заболевание получило название "фавизм". Недостаточность ацетилтрансферазы определяет снижение метаболизма противотуберкулезного препарата гидразида изоникотиновой кислоты, что обусловливает его плохую переносимость.
1.5. Побочное действие лекарственных средств
Согласно определению ВОЗ нежелательной считается любая реакция на лекарственное средство, вредная для организма, которая возникает при его использовании в дозах, рекомендуемых для лечения, диагностики или профилактики заболевания.
Синонимами побочного действия (ПД) являются лекарственно-ассоциированные, лекарственно-обусловленные, или ятрогенные, заболевания.
ЛС используют для изменения функций клеток, органов и систем организма, т.е. для достижения фармакологического эффекта.
Фармакологический эффект ЛС, желательный с терапевтической точки зрения (в данной клинической ситуации), называют главным (терапевтическим) эффектом (действием).
Фармакотерапия всегда сопряжена с опасностью развития побочной реакции/побочного действия (ПР/ПД). Побочное действие (побочный эффект) обусловлено фармакологическими свойствами ЛС (например, атония кишечника при назначении атропина сульфата), но нежелательно с терапевтической точки зрения (т.е. в данной клинической ситуации) и наблюдается при применении ЛС в дозах, рекомендованных для медицинского применения. Побочная реакция (ПР) не зависит от фармакологических свойств ЛС (аллергические проявления и т.п.), т.е. она наблюдается в тех случаях, когда не может быть исключена причинно-следственная связь между этой реакцией и применением ЛС. ПР/ПД могут усугублять течение заболевания, приводить к увеличению сроков пребывания в стационаре, а в отдельных случаях способствовать летальному исходу.
Многие лекарственные средства, оказывая полезное терапевтическое действие, могут вызывать нежелательные реакции, в некоторых случаях приводящие к тяжелым осложнениям и даже летальному исходу. Еще Гиппократ и Гален призывали к осторожности при использовании лекарственных препаратов.
Побочные реакции возникают при приеме любых лекарственных препаратов. Их частота при амбулаторном лечении достигает 10-20 %; 0,5-5 % больных нуждаются в госпитализации для лечения осложнений, вызванных ЛС.
Существуют много классификаций побочных реакций, возникающих в результате применения ЛС и осложнений фармакотерапии. Однако ни одна из них не является совершенной.
В представленной ниже классификации выделяют 4 типа побочных эффектов.
1. Тип А— частые, предсказуемые реакции, связанные с фармакологической активностью ЛС, которые могут наблюдаться у любого индивидуума (токсичность, связанная с передозировкой; токсичность, связанная с лекарственными взаимодействиями; второстепенные побочные эффекты, например, седативный эффект антигистаминных ЛС; вторичные побочные эффекты, например, дисбактериоз при использовании антибиотиков).
2. Тип В— нечастые, непредсказуемые реакции, встречающиеся только у чувствительных людей (лекарственная непереносимость, идиосинкразия, гиперчувствительность, псевдоаллергические реакции).
3. Тип С — реакции, связанные с длительной терапией (лекарственная зависимость).
4. Тип D— канцерогенные, мутагенные и тератогенные эффекты ЛС.
В основу следующей классификации положен патогенетический принцип.
1. Побочные эффекты, связанные с фармакологическими свойствами лекарственных средств. Данный вид побочных реакций встречается наиболее часто, они возникают при применении препарата в терапевтической дозе. Например, трициклические антидепрессанты не только влияют на ЦНС, но и вызывают сухость во рту и двоение в глазах; изопреналин при применении в качестве бронхолитика вызывает развитие аритмий. При увеличении дозы лекарственных средств риск появления побочных реакций повышается.
2. Токсические осложнения, обусловленные абсолютной или относительной передозировкой лекарственных веществ. Многие препараты в больших дозах вызывают токсические реакции. Так, парентеральное введение больших доз пенициллина (более 200млн ЕД в сутки), особенно у больных с почечной недостаточностью, может вызвать летаргию, спутанность сознания, эпилептиформные приступы. Это может быть связано с гипонартиемией или с введением большого количества калия, содержащегося в препарате. Передозировка сердечными гликозидами приводит к нарушению ритма сердца (развитие брадикардии, нарушения со стороны ЦНС, ЖКТ и др.).
3. Вторичные эффекты, обусловленные нарушением иммунобиологических свойств организма (ослабление иммунных реакций, дисбактериоз, кандидамикоз). В результате применения антибиотиков или других противомикробных средств изменяется нормальная бактериальная флора организма, которая приводит к суперинфекции, дисбактериозу и/или кандидамикозу.
4. Аллергические (иммунологические) реакции замедленного и немедленного типов. Данный вид ПД относят к побочным реакциям, не связанным с дозой лекарственных веществ. В их основе лежат индивидуальные особенности организма — аллергия или генетически обусловленные нарушения в ферментных системах организма. Особенностью реакций этого вида является то, что их трудно предвидеть. Анафилактические реакции — реакции гиперчувствительности немедленного типа, связанные с продукцией IgЕ-антител. Цитотоксические и цитолитические реакции связаны с образованием IgG и IgМ-антител и реакцией комплемента. Они могут вызываться сульфаниламидами, барбитуратами, производными пиразолона и др. и проявляться гемолитической анемией, гранулоцитопенией, тромбоцитопенией, развитием нефрита, артрита, лимфаденопатии.
5. Идиосинкразия —реакция, связанная с различными дефектами ферментов. Идиосинкразия — генетически обусловленная патологическая реакция на определенный лекарственный препарат. Эта реакция характеризуется резко повышенной чувствительностью больного к соответствующему препарату с необычайно сильным и/или продолжительным эффектом. В основе идиосинкразии лежат реакции, обусловленные наследственными дефектами ферментных систем.
6. Синдром отмены, наблюдающийся после прекращения длительного лечения некоторыми лекарственными препаратами. Синдром отмены возникает при быстрой отмене препарата после длительного назначения (например, при применении глюкокортикоидов, β-адреноблокаторов, клофелина, Н2-гистаминоблокаторов и др.).
Возможны самые разнообразные клинические проявления побочного действия ЛС. Чаще всего встречаются зуд, лихорадка, тошнота, рвота, головокружение, головная боль, нейропсихические расстройства (глюкокортикоиды вызывают эйфорию, психозы, амфетамины — дезориентацию, спутанность сознания). Нередко возникают кожные сыпи.
ЛС могут повреждать печень путем непосредственного воздействия самого препарата или чаще его метаболитов (например, четыреххлористый углерод и изониазид) и посредством иммунологических реакций.
Некоторые ЛС могут вызывать альбуминурию, гематурию и даже канальцевый некроз (НПВП в сочетании с фуросемидом).
Под воздействием ЛС могут более тяжело протекать некоторые заболевания, выявляться латентно текущие патологические процессы.
Иногда ЛС могут вызывать патологические синдромы. Так, резерпин и аминазин могут вызвать паркинсонизм, а глюкокортикоиды — артериальную гипертензию, стероидный диабет.
Зависимость патологических изменений от приема лекарственного препарата может быть установлена, если препарат был назначен незадолго до их появления. Связь становится очевидной, если отмена препарата сопровождается исчезновением побочных реакций, а повторное его назначение приводит к их рецидиву.
В ряде случаев установить лекарственную этиологию патологического процесса нелегко, например, при лекарственном гепатите и нефрите. После отмены препарата симптомы этих заболеваний еще долго сохраняются.
В 1976 году Vеrе описал склонность ПР на ЛС маскировать первоначальные заболевания и обосновал 5 причин, нераспознания ПР.
1. ПР могут быть настолько необычными и неожиданными, что трудно заподозрить их связь с безвредными ЛС, которые принимают больные.
2. Вызываемые ЛС расстройства часто могут имитировать естественные заболевания.
3. ПР появляются с длительной отсрочкой.
Лекарство может вызывать рецидив заболевания или расстройства у чувствительных лиц.
Клиническая картина заболевания может быть настолько сложной, что вызываемые ЛС реакции проходят незамеченными.
В последние годы были уточнены основные факторы и причины возникновения ПР/ПД ЛС (Д.Р. Лоуренс, Н.П. Беннит, М. Дюкс, 1995).
Факторы, не связанные с действием ЛС:
* особенности организма больного (возраст, пол, генетические особенности, склонность к аллергическим реакциям, специфика течения заболевания, вредные привычки);
* внешние относительно больного факторы (врач, который проводит фармакотерапию, экология, условия труда и др.).
Факторы, связанные с ПД препаратов:
* особенности клинико-фармакологической характеристики ЛС;
* адекватность выбора препарата;
* метод применения препарата;
* взаимодействие ЛС при полипрагмазии.
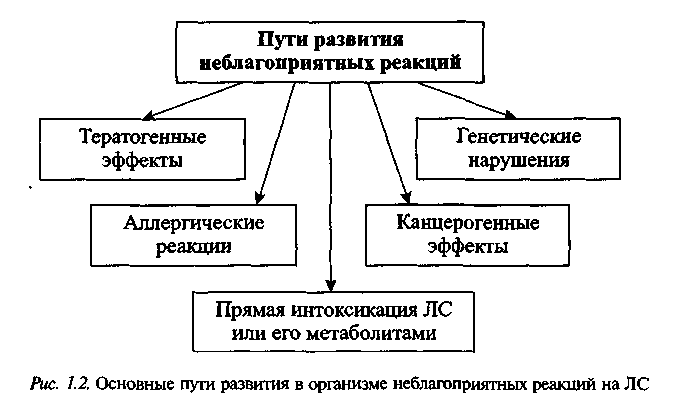
В настоящее время определены основные пути (рис. 1.2)/ развития неблагоприятных реакций со стороны ЛС (В.В. Чельцов, 1998; А.П. Викторов и соавт., 2001).
 |
1 2 3 4 5 6 7 8 9 ... 135